Положение галогенов в периодической таблице и строение их атомов. Хлор: физические и химические свойства, получение и применение.
План-конспект урока химии
Тема урока: Положение галогенов в периодической таблице и строение их атомов.
Хлор: физические и химические свойства, получение и применение.
Положение урока в теме. Урок «Положение галогенов в периодической таблице и строение их атомов. Хлор: физические и химические свойства, получение и применение» является первым в главе IX «ГАЛОГЕНЫ». Перед уроком учащимся задают повторить из гл. VI §36 (Периодическая таблица химических элементов) и из гл. VII §41(Основные виды химической связи) , §43(Степень окисления); ответить на вопрос – как с увеличением порядковых номеров изменяются свойства химических элементов в главных подгруппах периодической таблицы?
Цель урока. Обобщить и развить знания учащихся о строении атомов, свойствах химических элементов и их соединений в зависимости от положения в периодической таблице, строении молекул на примере галогенов. Изучить свойства хлора и его применение.
Задачи
обучения – обобщение и развитие знаний учащихся о строении атомов, свойствах химических элементов и их соединений в зависимости от положения в периодической таблице;
формирование новых понятий: о естественной группе галогенов, о свойствах хлора, элемента и вещества.
воспитания - формирование мировоззрения;
воспитание ответственности к работе;
развития - развитие речи учащихся;
развитие памяти учащихся;
развитие логического мышления учащихся
Методы урока:
наглядные (рассмотрение понятий темы, формул, рассмотрение протекания химических реакций, демонстрируемых учителем, применение медиапрезентации);
словесные (объяснения учителя и вопросы к классу).
Планируемые результаты обучения. Уметь давать характеристику элементов-галогенов по их положению в периодической таблице и строению атомов. Знать свойства хлора как простого вещества. Уметь составлять уравнения реакций, характеризующих химические свойства хлора.
Демонстрации. Получение хлора в лаборатории.
Ход урока:
-
Вводная часть.
Урок начинается рассмотрения темы и целей (слайд 1), короткой медиапрезентации галогенов (слайды 2-6). Учитель нацеливает учащихся на то, что на уроке ребята будут самостоятельно давать характеристику элементам подгруппы по заданному плану исходя только лишь из ее положения в ПСХЭ. Прежде чем ребята приступят к работе на доске составляют логическую цепь:
Положение в ПСХЭ→строение атома→строение электронной оболочки →свойства (слайд 7)
Учащиеся получают индивидуальные инструктирующие карты и приступают к выполнению заданий. (приложение 1 ), (приложение 2).
Далее совместно обсуждается каждый пункт предложенного плана, на интерактивной доске высвечиваются правильные ответы. (слайды 8-11)
После характеристики естественной группы галогенов, учитель сообщает о том, что наибольший практический интерес представляет хлор и его соединения. Класс приступает к рассмотрению свойств хлора. (слайд 12).
Демонстрационный опыт. Получение хлора. Рассмотрение уравнения реакции с точки зрения окислительно-восстановительных процессов.
Учащиеся отмечают физические свойства хлора, которые можно было наблюдать в ходе опыта.
Учитель дополняет (слайды 13,14), акцентирует внимание на мерах безопасности при работе с ядовитым газом. Заинтересованные учащиеся получают задание (по желанию) составить сообщения о ОВ, о загрязнении окружающей среды соединениями хлора, составить уравнения реакций взаимодействия хлора с растворами сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3, лежащих в основе кратковременной защиты органов дыхания.
Слайд 15 высвечивает план рассмотрения химических свойств хлора. В ходе выполнения задания учащиеся убеждаются в правильности предположения о том, что хлор чаще будет проявлять свойства окислителя.
Для тех ребят, кто справился с заданиями раньше других, дается творческое задание « Озвучь-ка». Предлагается самостоятельно рассмотреть механизм цепной реакции и озвучить динамическую схему механизма на интерактивной доске ( слайды 21,22).
Завершающее урок тестирование помогает закрепить приобретенные знания и умения.
Подведение итогов урока. Выставление оценок, комментирование их. Объявление домашнего задания. Рефлексия.
Тема урока: Положение галогенов в периодической таблице и строение их атомов.
Хлор: физические и химические свойства, получение и применение.
|
Учебный элемент |
Деятельность учителя |
Деятельность учащихся |
|
УЭ-0 |
И н т е г р и р у ю щ а я ц е л ь. Обобщить знания о строении атомов, свойствах химических элементов и их соединений в зависимости от положения в периодической таблице, строении молекул на примере галогенов. Изучить свойства хлора и его применение. |
|
|
Озвучивается тема и цель урока (слайд №1) |
|
|
|
УЭ-1. Актуализация опорных знаний. |
Медиапредставление галогенов (краткое) (слайды 2-6) .
Предложение
познакомиться с яркими представителями
подгруппы поближе через заполнение
таблицы «Характеристика
галогенов по положению Ц е л ь. Развивать умение учащихся давать характеристику элементов-галогенов по их положению в периодической таблице и строению атомов. При совместном обсуждении используются слайды 8-11 . |
1. Определение номера варианта. 2. Получение у учителя карточки в соответствии с номером своего варианта ( 1, 2 ) . 3.Выполнение заданий 1,2. (индивидуально и в парах) 4.Совместное обсуждение учащимися(фронтальная работа) характеристики подгруппы элементов по плану, дополнение, коррекция кратких записей в тетрадях. План изучения подгруппы элементов:
5. Выполнение задания 3 . |
|
УЭ-2. Организация восприятия материала |
Слайд 12. После выполнения этих заданий следует остановиться на элементе хлоре, так как он имеет наибольшее практическое значение из всех галогенов. Изучение свойств хлора как химического элемента и как простого вещества позволяет показать, что возможные формы существования химического элемента определяются строением его атома. |
Запись подзаголовка в тетрадях. Учащиеся дают характеристику хлору по положению в периодической таблице, используя общий план, и предсказывают его свойства. |
|
УЭ-3. Восприятие и осознание учебной информации |
Учитель демонстрирует получение хлора в лаборатории:
4НСl + MnО2 → MnСl2 + Сl2 ↑ + 2Н2О Рассказ о физических свойствах хлора (слайды 13,14). Высвечивание слайда 15.
При возникновении вопросов возможно совместное рассмотрение той или иной реакции ( быстрый переход по гиперссылке к конкретному уравнению, слайды 16-20)
|
Выполнение заданий 6-8. |
|
УЭ-3. Закрепление изученного материала |
Т е с т |
Выполни любые пять заданий теста, если считаешь, что можешь сделать больше, попробуй сделать еще. Работу выполняй под копирку. Один экземпляр сдай учителю, второй проверь сам по ключу, взятому у учителя, и поставь оценку. За 5 правильных ответов – «5». За 4 правильных ответа – «4». За 3 правильных ответа – «3». Если не набралось и трех баллов, подумай, в чем причина и как ее устранить Учащиеся тестируются. |
|
УЭ-4. Подведение итогов |
Человек рождается на свет, Чтоб творить, дерзать – и не иначе, Чтоб оставить в жизни добрый след И решить все трудные задачи. Человек рождается на свет... Для чего? Ищите свой ответ. Выставление оценок. Домашнее задание (слайд 23) Рефлексия |
Дети отвечают на вопросы: Р е ф л е к с и я. Учащиеся отвечают на вопросы. 1. Что, по-твоему, нам на уроке удалось? 2. Что необходимо сделать, чтобы ликвидировать имеющиеся проблемы и пробелы? 3. Чем ты был сегодня удивлен? |
Контрольные вопросы к уроку-семинару.
1. Как расположены элементы-неметаллы в периодической системе химических элементов?
2. Каковы особенности строения атомов неметаллов?
3. Какую роль – окислителя или восстановителя – выполняют элементы-неметаллы в химических реакциях?
4. От чего зависит степень окисления неметалла в соединении?
5. Каковы общие физические свойства неметаллов?
6. Какие связи могут образовывать атомы неметаллов в соединениях?
7. Какие элементы составляют семейство галогенов? Почему они так называются?
8. Каковы особенности строения атомов галогенов?
9. Каков химический характер галогенов, их возможные степени окисления?
10. Назовите природные соединения хлора.
11. Каковы физические свойства хлора?
12. Как получить хлорную воду?
13. Как получают хлор в промышленности и в лаборатории? Приведите соответствующие уравнения реакций.
14. Каковы химические свойства хлора? Приведите уравнения реакций.
15. Что происходит с хлорной водой на свету? Запишите уравнение химической реакции.
16. Почему хлор может вытеснять бром и йод из растворов их солей?
17. Как хлор взаимодействует со щелочами?
18. Каковы формулы высших оксида и гидроксида хлора?
19. Как ведет себя бертолетова соль при нагревании? Запишите уравнение реакции.
20. Как хлор может спасти от отравления?
21. Каково биологическое действие хлора?
22. Какого типа связи образует хлор в своих соединениях? Приведите примеры.
23. Каковы физические свойства хлороводорода?
24. Что получается при растворении хлороводорода в воде?
25. Как можно получить хлороводород? Составьте соответствующие уравнения реакций.
26. Каковы химические свойства соляной кислоты? Напишите уравнения реакций.
27. Как распознать соляную кислоту и ее соли? Приведите уравнения качественных реакций.
28. Где применяются соляная кислота и хлориды?
29. Как правильно растворять хлороводород в воде?
30. Почему фтор является самым активным неметаллом?
31. Назовите важнейшие минералы, содержащие фтор.
32. Каковы физические свойства фтора?
33. Как можно получить фтор? Напишите уравнение реакции.
34. Каковы химические свойства фтора? Напишите уравнения реакций.
35. Как можно получить фтороводород? Каковы его физические свойства?
36. Как называется раствор фтороводорода в воде?
37. Каковы особые химические свойства плавиковой кислоты?
38. Где применяются фтор и его соединения?
39. Где в природе встречаются бром и йод?
40. Как можно получить в чистом виде бром и йод? Напишите уравнения реакций.
41. Каковы химические свойства брома и йода? Есть ли различия? Подтвердите свой ответ уравнениями реакций.
42. Каковы качественные реакции на ионы брома и йода? Приведите уравнения реакций.
43. Как уберечься от ожогов бромом?
44. Где применяются бром, йод и их соединения?
Задания для самоконтроля
1. Расставьте коэффициенты в приведенных схемах окислительно-восстановительных реакций методом электронного баланса.
а) Cl2 + Вr2 + Н2О → НВrO3 + НСl;
б) Сl2 + Н2S +Н2O→ Н2SO4 + НСl;
в) КСlO4 + Аl + H2SO4 → Al2(SO4)3 + KCl + Н2О;
г) КСlO3 + МnCl2 + КОН → МnО2 + КСl + Н2О;
д) СrCl3 + NaClO + NaОН → Na2СrО4 + NaCl + Н2О.
2. С какими из перечисленных ниже веществ реагирует соляная кислота: хлорид кальция, медь, сульфат натрия, сульфат бария, гидроксид калия, оксид магния, алюминий, нитрат серебра, карбонат кальция? Запишите уравнения возможных реакций. Расставьте коэффициенты (для окислительно-восстановительных реакций методом электронного баланса).
3. Напишите уравнения реакций, которые нужно провести для осуществления следующих превращений:
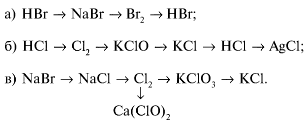
Задания для самоконтроля
1. Определите объем (н. у.), который займет хлор:
а) массой 14,2 г;
б) количеством вещества 2 моль;
в) числом молекул, равным 3,01•1023.
Ответ. а) 4,48 л; б) 44,8 л; в) 11,2 л.
2. Определите молярную массу галогена и сам галоген, если 1 л (н. у.) его имеет массу 1,696 г.
Ответ. F2.
3. Найдите массу смеси, состоящей из 5,6 л хлора и 33,6 л хлороводорода. Каково содержание веществ в этой смеси в процентах по объему?
Ответ. 72,5 г,φ(Cl2) = 14,3%, φ(НCl) = 85,7%.
4. Определите максимальный объем хлороводорода, который может образоваться при реакции 3,01•1023 молекул водорода и 35,5 г хлора.
Ответ. 22,4 л (н. у.).
5. Сколько миллилитров раствора соляной кислоты с концентрацией 2 моль/л окислилось оксидом марганца(IV), если известно, что выделенный при этом хлор может вытеснить из раствора йодида калия 25,4 г йода.
Ответ. 200 мл.
6. Какую массу оксида марганца(IV) и какой объем раствора соляной кислоты с плотностью
1,18 г/мл и массовой долей НСl 36% надо взять для получения хлора, который может вытеснить из раствора йодида калия 30,48 г молекулярного йода. Считать выход продуктов на каждой из стадий процесса равным 80% от теоретически возможного.
Ответ. 64,4 мл соляной кислоты и 16,3 г MnO2.
7. 800 г хлорида натрия обработали концентрированной серной кислотой и выделившийся газ пропустили через воду. Определите выход в реакции, если получен 1 л 20%-го раствора соляной кислоты с плотностью 1,1 кг/дм3.
Ответ. 44%.
8. При действии на 261 г смеси хлоридов натрия и калия избытка концентрированной серной кислоты получено 89,6 л хлороводорода. Определите состав смеси в процентах по массе.
Ответ. ω(NaCl) = 51,6%, ω(KCl) = 48,4%.
Ответы на задания для самоконтроля
3.3. Некоторые соединения галогенов и их свойства
1.
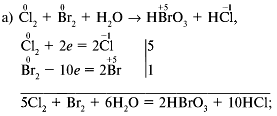
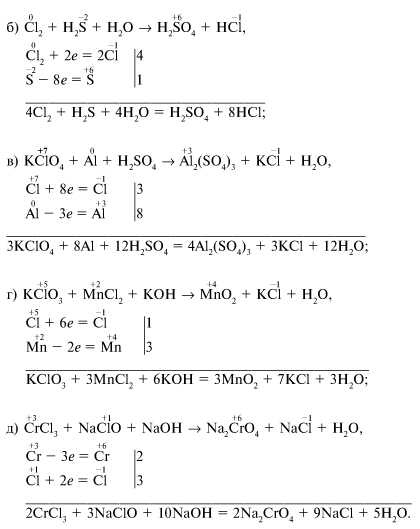
2. Из заданных веществ соляная кислота реагирует со следующими:
HCl + KOH = KCl + H2O;
2HCl + MgO = MgCl2 + H2O;
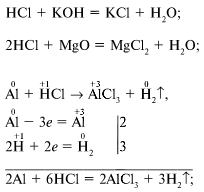
HCl + AgNO3 = AgCl↓ + HNO3;
2HCl + CaCO3 = CaCl2 + H2O + CO2↑.
3. Уравнения реакций для цепочек химических превращений
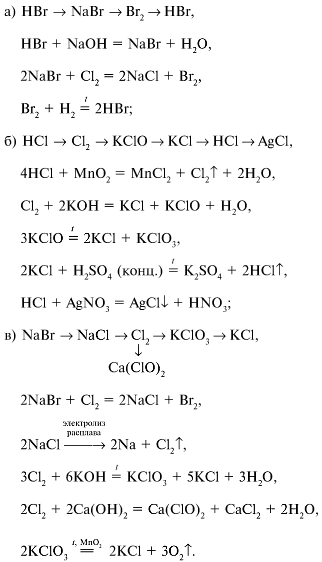
Тема урока: Положение галогенов в периодической таблице и строение их атомов.
Хлор: физические и химические свойства, получение и применение.
1 вариант.
-
Запиши в тетради дату и тему урока.
-
Пользуясь учебником §46 (с. 157) и планом изучения подгруппы элементов обсудите и составьте с напарником характеристику элементов-галогенов по их положению в периодической таблице и строению атомов. Сделайте краткую запись в тетради по каждому пункту плана чернилами красного цвета.
. План изучения подгруппы элементов:
1. Положение подгруппы в периодической системе химических элементов (далее – ПСХЭ): номер группы – главная или побочная.
2. Состав подгруппы (выписать символы и названия химических элементов).
-
Строение атомов элементов (для каждого элемента записать формулу состава атома ((___p+,___ no )___ e- )), распределение электронов по энергетическим уровням, электронную конфигурацию валентного слоя атома).
-
Сходство в строении атомов элементов подгруппы.
-
Отличие в строении атомов элементов.
-
Свойства элементов подгруппы (металлы или неметаллы).
-
Возможные степени окисления элементов подгруппы.
-
Строение молекул.
-
Сравнение свойств элементов в подгруппе ( как изменяются атомный радиус, химическая активность и окислительные свойства элементов в подгруппе).
3. Активно участвуйте в совместном обсуждении характеристики элементов-галогенов по их положению в периодической таблице и строению атомов Внесите дополнения, исправьте ошибки чернилами синего цвета.
4. Запишите подзаголовок .
Хлор: физические и химические свойства, получение и применение
5. Дайте характеристику хлору по положению в периодической таблице, используя общий план, и предскажите его свойства.
6.Посмотрите демонстрационный опыт. Запишите уравнение реакции, разберите эту реакцию с точки зрения процессов окисления и восстановления.
7. Кратко запишите физические свойства хлора, обратите внимание на меры предосторожности при работе с веществом.
8. Рассмотрите химические свойства хлора с помощью § 47,выполните необходимые записи. Разберите реакции с точки зрения процессов окисления и восстановления. Сделайте выводы о химических свойствах хлора.
9.* Рассмотрите механизм цепной реакции (с.162). Попробуйте озвучить динамическую схему механизма на интерактивной доске ( слайды 21,22).
10. По рисунку 73 ( с.163) проследи области применения хлора.
11. Ответь на вопросы теста.
1 вариант
А-1. К группе VIIА периодической системы химических элементов не относится атом, имеющий строение электронной оболочки
1) 2,8,7 2)2,7 3)2,5 4)2,8,18,7
А-2. В ряду I 2 → Br 2 → Cl 2 → F 2 неметаллические свойства простых веществ, образованных химическими элементами,
1) не изменяются
2) сначала усиливаются, затем ослабевают
3) усиливаются
4) ослабевают
А-3.В чем различие в строении атомов галогенов?
1) заряд ядра атома
2) радиус атома
3) наружный электронный слой близок к завершенному
4) относительная атомная масса
А-4. Как изменяется электроотрицательность в группе галогенов?
1) ЭO(F) > ЭО(Cl) > ЭО(Br) > ЭО(I)
2) ЭO(F) = ЭО(Сl) = ЭО(Br) = ЭО(I)
3) ЭО(I) > ЭО(Br) > ЭО(Cl) > ЭО(F)
4) ЭО(F) < ЭО(Сl) = ЭО(Br) > ЭO(I)
А-5. Галогены являются
1) сильными восстановителями
2) сильными окислителями
3) переходными элементами
4) как восстановителями, так и окислителями
А-6. Галогены — простые вещества — имеют одинаковый вид химической связи, удерживающей атомы в молекулах, и одинаковый тип кристаллической решетки, но разное агрегатное состояние. Это объясняется тем, что
1) в узлах кристаллической решетки находятся одинаковые по массе частицы, но расположенные друг от друга на разном расстоянии
2) в узлах кристаллической решетки находятся двухатомные молекулы с разной массой и разной силой притяжения
3) в узлах кристаллической решетки находятся нейтральные атомы, на которые не действуют силы межатомного (межмолекулярного) притяжения в кристалле
4) галогены образуют кристаллы разной формы
А-7.Галогены в своих соединениях могут проявлять переменную степень окисления. Выберите правильные ответы.
|
Вещества |
Степени окисления галогенов |
|
1. F2, HF, O2F, CaF2 |
A. 0, –1, +5, +3 |
|
2. Br2, HBr, Br2O5, Br2O3 |
Б. 0, –1, +7, –1 |
|
3. Cl2, HCl, Cl2O7, HClO4 |
В. 0, –1, –1, –1 |
|
|
Г. 0, –1, +7, +7 |
А-8. Вид химической связи в соединениях, образованных галогенами, неодинаков. Выберите правильные ответы
|
Соединения галогенов |
Вид химической связи |
|
1. Молекулы простых веществ (F2, Сl2, Br2, I2) |
А. Ковалентная полярная |
|
2. Летучие водородные соединения |
Б. Металлическая |
|
3. Соли (NaCl, KBr, CuI2, CaF2) |
В. Ковалентная неполярная |
|
|
Г. Ионная |
А-9. Галогены и их соединения в твердом состоянии имеют кристаллическое строение. Какой тип кристаллической решетки можно предположить у галогенов и образованных ими веществ, находящихся в твердом состоянии? Выберите правильный ответ.
|
Соединения |
Тип кристаллической решетки |
|
1. Галогены — простые вещества |
А. Ионная |
|
2. Галогеноводороды |
Б. Атомная |
|
3. Соли бескислородных кислот (растворов галогеноводородов) |
В. Молекулярная |
|
|
Г. Металлическая |
Тема урока: Положение галогенов в периодической таблице и строение их атомов.
Хлор: физические и химические свойства, получение и применение.
2 вариант.
-
Запиши в тетради дату и тему урока.
-
Пользуясь учебником §46 (с. 157) и планом изучения подгруппы элементов обсудите и составьте с напарником характеристику элементов-галогенов по их положению в периодической таблице и строению атомов. Сделайте краткую запись в тетради по каждому пункту плана чернилами красного цвета.
. План изучения подгруппы элементов:
1. Положение подгруппы в периодической системе химических элементов (далее – ПСХЭ): номер группы – главная или побочная.
2. Состав подгруппы (выписать символы и названия химических элементов).
-
Строение атомов элементов (для каждого элемента записать формулу состава атома ((___p+,___ no )___ e- )), распределение электронов по энергетическим уровням, электронную конфигурацию валентного слоя атома).
-
Сходство в строении атомов элементов подгруппы.
-
Отличие в строении атомов элементов.
-
Свойства элементов подгруппы (металлы или неметаллы).
-
Возможные степени окисления элементов подгруппы.
-
Строение молекул.
-
Сравнение свойств элементов в подгруппе ( как изменяются атомный радиус, химическая активность и окислительные свойства элементов в подгруппе).
3. Активно участвуйте в совместном обсуждении характеристики элементов-галогенов по их положению в периодической таблице и строению атомов Внесите дополнения, исправьте ошибки чернилами синего цвета.
4. Запишите подзаголовок .
Хлор: физические и химические свойства, получение и применение
5. Дайте характеристику хлору по положению в периодической таблице, используя общий план, и предскажите его свойства.
6.Посмотрите демонстрационный опыт. Запишите уравнение реакции, разберите эту реакцию с точки зрения процессов окисления и восстановления.
7. Кратко запишите физические свойства хлора, обратите внимание на меры предосторожности при работе с веществом.
8. Рассмотрите химические свойства хлора с помощью § 47,выполните необходимые записи. Разберите реакции с точки зрения процессов окисления и восстановления. Сделайте выводы о химических свойствах хлора.
9.* Рассмотрите механизм цепной реакции (с.162). Попробуйте озвучить динамическую схему механизма на интерактивной доске ( слайды 21,22).
10. По рисунку 73 ( с.163) проследи области применения хлора.
11. Ответь на вопросы теста.
2вариант
А-1. К группе VIIА периодической системы химических элементов относится атом, имеющий строение электронной оболочки
1) 2,6 2) 2,8,18,5 3)2,8,1 4) 2,8,7
А-2. В ряду I 2 → Br 2 → Cl 2 → F 2 окислительные свойства простых веществ, образованных химическими элементами,
1) не изменяются
2) сначала усиливаются, затем ослабевают
3) усиливаются
4) ослабевают
А-3. Особенности в строении атомов галогенов, обусловливающие их принадлежность к типичным неметаллам
1) заряд ядра атома
2) радиус атома
3) общее число электронов, вращающихся вокруг ядра атома
4) близкое к завершению общее число электронов, находящихся на наружном электронном слое атома, и способность атома легко принимать недостающие для этого электроны
А-4. Как изменяется электроотрицательность в группе галогенов?
1) ЭO(F) > ЭО(Cl) > ЭО(Br) > ЭО(I)
2) ЭO(F) = ЭО(Сl) = ЭО(Br) = ЭО(I)
3) ЭО(I) > ЭО(Br) > ЭО(Cl) > ЭО(F)
4) ЭО(F) < ЭО(Сl) = ЭО(Br) > ЭO(I)
А-5. Галогены являются
1) сильными восстановителями
2) сильными окислителями
3) переходными элементами
4) как восстановителями, так и окислителями
А-6. Галогены — простые вещества — имеют одинаковый вид химической связи, удерживающей атомы в молекулах, и одинаковый тип кристаллической решетки, но разное агрегатное состояние. Это объясняется тем, что
1) в узлах кристаллической решетки находятся одинаковые по массе частицы, но расположенные друг от друга на разном расстоянии
2) в узлах кристаллической решетки находятся двухатомные молекулы с разной массой и разной силой притяжения
3) в узлах кристаллической решетки находятся нейтральные атомы, на которые не действуют силы межатомного (межмолекулярного) притяжения в кристалле
4) галогены образуют кристаллы разной формы
А-7.Галогены в своих соединениях могут проявлять переменную степень окисления. Выберите правильные ответы.
|
Вещества |
Степени окисления галогенов |
|
1. F2, HF, O2F, CaF2 |
A. 0, –1, +5, +3 |
|
2. I2, HI, I2O7, KI |
Б. 0, –1, +7, –1 |
|
3. Cl2, HCl, Cl2O7, HClO4 |
В. 0, –1, –1, –1 |
|
|
Г. 0, –1, +7, +7 |
А-8. Вид химической связи в соединениях, образованных галогенами, неодинаков. Выберите правильные ответы
|
Соединения галогенов |
Вид химической связи |
|
1. Молекулы простых веществ (F2, Сl2, Br2, I2) |
А. Ковалентная полярная |
|
2. Летучие водородные соединения |
Б. Металлическая |
|
3. Соли (NaCl, KBr, CuI2, CaF2) |
В. Ковалентная неполярная |
|
|
Г. Ионная |
А-9. Галогены и их соединения в твердом состоянии имеют кристаллическое строение. Какой тип кристаллической решетки можно предположить у галогенов и образованных ими веществ, находящихся в твердом состоянии? Выберите правильный ответ.
|
Соединения |
Тип кристаллической решетки |
|
1. Галогены — простые вещества |
А. Ионная |
|
2. Галогеноводороды |
Б. Атомная |
|
3. Соли бескислородных кислот (растворов галогеноводородов) |
В. Молекулярная |
|
|
Г. Металлическая |
1 вариант
А-1. К группе VIIА периодической системы химических элементов не относится атом, имеющий строение электронной оболочки
1) 2,8,7 2)2,7 3)2,5 4)2,8,18,7
А-2. В ряду I 2 → Br 2 → Cl 2 → F 2 неметаллические свойства простых веществ, образованных химическими элементами,
1) не изменяются
2) сначала усиливаются, затем ослабевают
3) усиливаются
4) ослабевают
А-3.В чем различие в строении атомов галогенов?
1) заряд ядра атома
2) радиус атома
3) наружный электронный слой близок к завершенному
4) относительная атомная масса
А-4. Как изменяется электроотрицательность в группе галогенов?
1) ЭO(F) > ЭО(Cl) > ЭО(Br) > ЭО(I)
2) ЭO(F) = ЭО(Сl) = ЭО(Br) = ЭО(I)
3) ЭО(I) > ЭО(Br) > ЭО(Cl) > ЭО(F)
4) ЭО(F) < ЭО(Сl) = ЭО(Br) > ЭO(I)
А-5. Галогены являются
1) сильными восстановителями
2) сильными окислителями
3) переходными элементами
4) как восстановителями, так и окислителями
А-6. Галогены — простые вещества — имеют одинаковый вид химической связи, удерживающей атомы в молекулах, и одинаковый тип кристаллической решетки, но разное агрегатное состояние. Это объясняется тем, что
1) в узлах кристаллической решетки находятся одинаковые по массе частицы, но расположенные друг от друга на разном расстоянии
2) в узлах кристаллической решетки находятся двухатомные молекулы с разной массой и разной силой притяжения
3) в узлах кристаллической решетки находятся нейтральные атомы, на которые не действуют силы межатомного (межмолекулярного) притяжения в кристалле
4) галогены образуют кристаллы разной формы
А-7.Галогены в своих соединениях могут проявлять переменную степень окисления. Выберите правильные ответы.
|
Вещества |
Степени окисления галогенов |
|
1. F2, HF, O2F, CaF2 |
A. 0, –1, +5, +3 |
|
2. Br2, HBr, Br2O5, Br2O3 |
Б. 0, –1, +7, –1 |
|
3. Cl2, HCl, Cl2O7, HClO4 |
В. 0, –1, –1, –1 |
|
|
Г. 0, –1, +7, +7 |
А-8. Вид химической связи в соединениях, образованных галогенами, неодинаков. Выберите правильные ответы
|
Соединения галогенов |
Вид химической связи |
|
1. Молекулы простых веществ (F2, Сl2, Br2, I2) |
А. Ковалентная полярная |
|
2. Летучие водородные соединения |
Б. Металлическая |
|
3. Соли (NaCl, KBr, CuI2, CaF2) |
В. Ковалентная неполярная |
|
|
Г. Ионная |
А-9. Галогены и их соединения в твердом состоянии имеют кристаллическое строение. Какой тип кристаллической решетки можно предположить у галогенов и образованных ими веществ, находящихся в твердом состоянии? Выберите правильный ответ.
|
Соединения |
Тип кристаллической решетки |
|
1. Галогены — простые вещества |
А. Ионная |
|
2. Галогеноводороды |
Б. Атомная |
|
3. Соли бескислородных кислот (растворов галогеноводородов) |
В. Молекулярная |
|
|
Г. Металлическая |
2вариант
А-1. К группе VIIА периодической системы химических элементов относится атом, имеющий строение электронной оболочки
1) 2,6 2) 2,8,18,5 3)2,8,1 4) 2,8,7
А-2. В ряду I 2 → Br 2 → Cl 2 → F 2 окислительные свойства простых веществ, образованных химическими элементами,
1) не изменяются
2) сначала усиливаются, затем ослабевают
3) усиливаются
4) ослабевают
А-3. Особенности в строении атомов галогенов, обусловливающие их принадлежность к типичным неметаллам
1) заряд ядра атома
2) радиус атома
3) общее число электронов, вращающихся вокруг ядра атома
4) близкое к завершению общее число электронов, находящихся на наружном электронном слое атома, и способность атома легко принимать недостающие для этого электроны
А-4. Как изменяется электроотрицательность в группе галогенов?
1) ЭO(F) > ЭО(Cl) > ЭО(Br) > ЭО(I)
2) ЭO(F) = ЭО(Сl) = ЭО(Br) = ЭО(I)
3) ЭО(I) > ЭО(Br) > ЭО(Cl) > ЭО(F)
4) ЭО(F) < ЭО(Сl) = ЭО(Br) > ЭO(I)
А-5. Галогены являются
1) сильными восстановителями
2) сильными окислителями
3) переходными элементами
4) как восстановителями, так и окислителями
А-6. Галогены — простые вещества — имеют одинаковый вид химической связи, удерживающей атомы в молекулах, и одинаковый тип кристаллической решетки, но разное агрегатное состояние. Это объясняется тем, что
1) в узлах кристаллической решетки находятся одинаковые по массе частицы, но расположенные друг от друга на разном расстоянии
2) в узлах кристаллической решетки находятся двухатомные молекулы с разной массой и разной силой притяжения
3) в узлах кристаллической решетки находятся нейтральные атомы, на которые не действуют силы межатомного (межмолекулярного) притяжения в кристалле
4) галогены образуют кристаллы разной формы
А-7.Галогены в своих соединениях могут проявлять переменную степень окисления. Выберите правильные ответы.
|
Вещества |
Степени окисления галогенов |
|
1. F2, HF, O2F, CaF2 |
A. 0, –1, +5, +3 |
|
2. I2, HI, I2O7, KI |
Б. 0, –1, +7, –1 |
|
3. Cl2, HCl, Cl2O7, HClO4 |
В. 0, –1, –1, –1 |
|
|
Г. 0, –1, +7, +7 |
А-8. Вид химической связи в соединениях, образованных галогенами, неодинаков. Выберите правильные ответы
|
Соединения галогенов |
Вид химической связи |
|
1. Молекулы простых веществ (F2, Сl2, Br2, I2) |
А. Ковалентная полярная |
|
2. Летучие водородные соединения |
Б. Металлическая |
|
3. Соли (NaCl, KBr, CuI2, CaF2) |
В. Ковалентная неполярная |
|
|
Г. Ионная |
А-9. Галогены и их соединения в твердом состоянии имеют кристаллическое строение. Какой тип кристаллической решетки можно предположить у галогенов и образованных ими веществ, находящихся в твердом состоянии? Выберите правильный ответ.
|
Соединения |
Тип кристаллической решетки |
|
1. Галогены — простые вещества |
А. Ионная |
|
2. Галогеноводороды |
Б. Атомная |
|
3. Соли бескислородных кислот (растворов галогеноводородов) |
В. Молекулярная |
|
|
Г. Металлическая |
- Психология профессионального образования: общая характеристика
- Вебинар «Развитие интеллектуальных и творческих способностей дошкольников через моделирование и конструирование: палочки Кюизенера, блоки Дьенеша, Дары Фрёбеля»
- Международный вебинар «Нейроигры и нейроупражнения как средство формирования межполушарного взаимодействия, коррекции и развития интеллектуальных возможностей у дошкольников»
- Международный вебинар «Социально-культурные основы занятий физической культурой и спортом»
- Международный вебинар «Функциональный подход и его преимущества в помощи детям младенческого и раннего возраста с ОВЗ, включая детей-инвалидов»
- Вебинар «Мы читаем по слогам: развивающие игры, задания и упражнения для детей 5 – 7 лет (разрезные картинки, кубики, слоговое домино и лото)»






