Химические свойства спиртов
«Химические свойства спиртов»
Презентация к уроку по теме "Химические свойства спиртов" с возможностью индивидуального обучения и использования ТКМ. Содержит видеоролики ЕКОР. Презентация состоит из двух модулей. Первый модуль может быть использован при проведении урока по химии в 10-м классе с использованием ТКМ (запускается на рабочем месте учителя). Второй модуль может быть использован при проведении занятия в компьютерном классе (запускается на рабочих местах учащихся) или индивидуальной работе учащихся. Деление на модули происходит на первом слайде презентации. Кнопка «ПРЕЗЕНТАЦИЯ» запускает первый модуль – линейную презентацию к уроку. Кнопка «ИНДИВИДУАЛЬНОЕ ОБУЧЕНИЕ» запускает второй обучающий модуль.
Класс разбивается на 4-ре группы и каждой ставится задача:
1 Ваша задача в предложенном материале, выбирать самое главное.
2. Ваша задача, опираясь на предыдущий опыт выбрать из предложенного материала то, что вам уже известно.
3 Ваша задача, опираясь на предыдущий опыт выбрать в предложенном материале, то, что вам ещё не встречалось и с чем вы ещё не знакомы.
4 Ваша основная задача – обобщать и делать выводы
Учащимся раздаются инструктивные карты. (приложение1.)
Химические свойства спиртов можно проиллюстрировать следующей схемой.
На основании своих целей каждая группа анализирует схему и делает выводы.
Дальнейшая работа идёт по схеме:
— Переход (вводная часть к химическому свойству)
— Просмотр видеоролика
— Работа в группах (анализ, кластер, выводы)
— Обсуждение и общий вывод.
Привожу полностью данную схему для первой реакции горения, а для остальных, только описание переходов.
В 1640 году Роберт Бойль, получая концентрированные растворы спиртов, предложил использовать их в качестве высококалорийного горючего. Роберт Бойль известен как замечательный экспериментатор, но, сколько открытий могли бы быть названы именем этого великого учёного, если бы он умел делать правильные выводы. Давайте мы с вами перенесёмся в современную лабораторию и, посмотрев, как горят спирты, научимся делать правильные выводы.
Просмотр видео ролика. Теперь давайте проанализируем процессы происходящие при горении спирта.
- какие вещества выделяются при горении спирта?
- Почему бутиловый и пентиловый спирты труднее зажечь?
- Почему при горении пентилового спирта выделяется копоть?
- Какова сумма коэффициентов в реакции горения? Обратить внимание!!!
А теперь давайте заполним кластеры «Горение спиртов»
Первая группа
n Что могут сказать по поводу данной реакции наши практики? Что происходит при горении спиртов?
nА что может сказать аналитическая группа? Что из приведённого нам уже было известно?
n Что нового вы узнали о горении спиртов?
От экспертной группы мы ждём заключительных выводов.Просмотр видео ролика.
При горении спирта выделяется 1370 кДж/моль энергии, а при метаболизме этанола в организме 770 кДж/моль
Вопрос: Откуда такая разница?
Ответ: В организме спирты окисляются до других органических соединений.
Об этом речь дальше.
Внимание на экран, смотрим видео ролик «Окисление спирта оксидом меди».
Реакцию окисления спирта мы можем представить следующим уравнением. Обратите внимание, спирты в данной реакции окисляются до альдегидов. Эти реакции идут в организме человека при выведении из него этанола. Чтобы получить смертельную дозу достаточно выпить 300 г. 96% спирта.
А теперь давайте перейдём к заполнению кластеров «Окисление спиртов».
Взаимодействие спиртов с натрием впервые наблюдал нмецкий химик-аналитик Юстус Либих. Однажды в 1833 году ему подарили партию хорошего вина изготовления 1811 г. Либиху это вино показалось кисловатым, и он обработал его натрием, после чего с восторгом отметил, что «вино приобрело мягкость, не потеряв ни одного из своих достоинств».
Либих посылает ящик вина, обработанного реактивами, Вёлеру, чтобы тот мог «насладиться его редкостью». В ответ он получил письмо: «Что касается подарка, то я благодарен тебе скорее за дружеские намерения, чем за само вино. Оно слишком старо и похоже по вкусу на лекарство». Неудача заставила Либиха заняться химизмом реакций взаимодействия спирта с натрием. А теперь давайте перенесёмся в современную лабораторию и посмотрим, как взаимодействуют спирты со щелочными металлами.
Клод-Луи Бертолле в 1799 году во время Египетской экспедиции Бонапарта Наблюдая за условиями образования соды в соляных озерах пришел к выводу, что направление химических реакций зависит от условий, в которых эти реакции протекают. Так было положено начало учения о химическом равновесии. Посмотрев следующий видео фрагмент, ответьте на вопрос:
Какие факторы используют для смещения равновесия в сторону образования бромэтана?
. Реакция замещения – это классический пример обратимой химической реакции.
— Давайте вспомним, какие факторы влияют на смещение химического равновесия?
— Как смещалось химическое равновесие в реакции образования бромэтана.
В 1275 г. Раймонд Луллиус
в 1540 г Валериус Кордус и вэтомже году Парацельсом
в 1680 г. Р.Бойль
в 1704 г Исаак Ньютон.
Что объединяет этих людей и эти даты, это – переоткрытие диэтилового эфира. Первенство в получении, которого, несомненно, принадлежит Валериусу Кордусу.
Решение заданий по теме.
Химические свойства спиртов
Ваша основная задача – обобщать и делать выводы
1. Прочтите текст и сделайте вывод на основе своих задач.
В гидроксогруппе связь полярная и при химических реакциях она может гетеролитически разрываться с образованием катиона водорода. Это обуславливает кислотные свойства спиртов. Атом углерода, связанный с гидроксильной группой, имеет дефицит электронной плотности, следовательно, он может быть объектом атаки нуклеофильным реагентом. При этом разрываться будет связь С-О, тип реакции – нуклеофильное замещение.
Вывод:_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
2.. Горение спиртов












С4Н9ОН + О2 =
3. Окисление спиртов
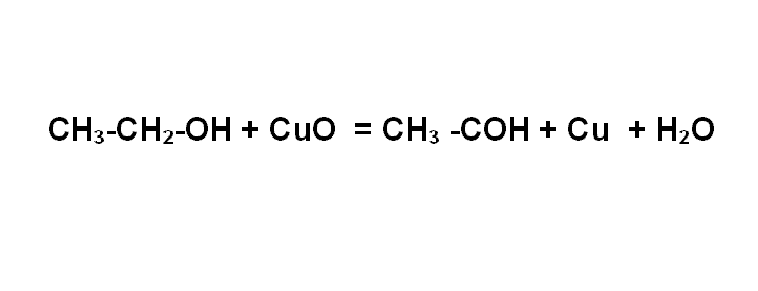









4. Кислотные свойства спиртов
![]()








5. Реакции замещения СН3СООН + С2Н5ОН ↔












6. Реакции дегидратации CH3-CH2-OH →








- Вебинар «Развитие интеллектуальных и творческих способностей дошкольников через моделирование и конструирование: палочки Кюизенера, блоки Дьенеша, Дары Фрёбеля»
- Международный вебинар «Нейроигры и нейроупражнения как средство формирования межполушарного взаимодействия, коррекции и развития интеллектуальных возможностей у дошкольников»
- Психология профессионального образования: общая характеристика
- Международный вебинар «Функциональный подход и его преимущества в помощи детям младенческого и раннего возраста с ОВЗ, включая детей-инвалидов»
- Международный вебинар «Обучение грамоте старших дошкольников с помощью развивающих игр В. В. Воскобовича: практика реализации ФГОС и ФОП ДО»
- Международный вебинар «Просвещение родителей (законных представителей) по вопросам здоровья, воспитания и развития детей раннего и дошкольного возраста: приемы, средства и формы»






